2022年09月26日(东京)第一三共(Daiichi Sankyo)宣布日本厚生劳动省已经批准了EZHARMIA(Valemetostat tosilate)的上市申请,用于治疗复发或难治性T细胞白血病/淋巴瘤(ALT)成人患者。
- Ezharmia ( valemetostat)是第1个获得监管批准的治疗ATL的EZH1和 EZH2双重抑制剂.
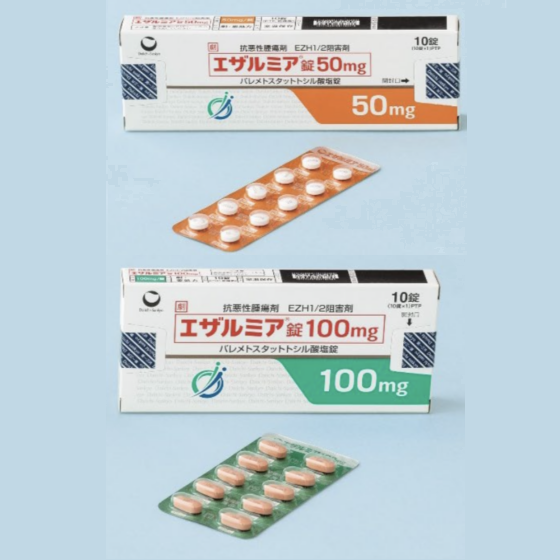
此次批准主要基于一项开放标签、单臂的II期研究的结果,该研究评估了Valemetostat在25例复发或难治性ATL的侵略性亚型患者中的有效性和安全性,这些患者既往接受过莫格利珠单抗或至少一次系统化疗治疗。
经独立疗效评估委员会评估,患者的客观缓解率(ORR)为48%(95%CI:27.8%-68.7%),其中20%的患者(n=5)获得了完全缓解(CR),28%的患者(n=7)实现部分缓解(PR),研究达到主要终点。
总体上,Valemetostat的安全性和耐受性良好,最常见的不良反应包括血小板计数减少(80%)、贫血(44%)、脱发(40%)和痛风(36%)等。
EZHARMIA(Valemetostat) (DS-3201, DS-3201b) 是一款first-in-class的靶向EZH1和EZH2的双重抑制剂。EZH1和EZH2通过参与组蛋白甲基化发挥作用,以调节造血干细胞相关的基因表达。研究发现,这两种酶常在血液学恶性肿瘤(包括一些T细胞淋巴瘤)中发生突变或过度表达。
成人T细胞白血病/淋巴瘤 (Adult T-cell leukemia/lymphoma,ATL) 是一种罕见的侵袭性外周T细胞淋巴瘤 (PTCL),由人类T细胞嗜淋巴细胞病毒 1 型 (HTLV-1) 引起。
全世界每年诊断出超过3,000例新的ATL病例。ATL 在 HTLV-1 病毒流行的地区发生频率更高,包括日本西南部、中南美洲和澳大利亚中部。在北美和欧洲也观察到病例,非流行地区的 ATL 发病率正在上升。在日本,每年约有 1,000 例新的 ATL 病例和超过 1,000 例 ATL 死亡。与其他类型的 PTCL 相比,ATL 的预后最差,五年总生存率约为 14%。据报道,日本最常见的急性 ATL 亚型患者的中位生存时间约为8个月(252 天)。ATL的治疗基于亚型,主要包括强化多药化疗方案。近 90% 的患者在完成强化一线治疗后会复发,此时可用的选择很少。需要额外的治疗来改善日本和世界范围内 ATL 的预后。
| 信息 | 来源 |
| EZHARMIA® Approved in Japan as First Dual EZH1 and EZH2 Inhibitor Therapy for Patients with Adult T-Cell Leukemia/ Lymphoma | https://www.daiichisankyo.com/files/news/pressrelease/pdf/202209/20220926_E.pdf |
| 免责声明 | 本资料仅作参考,诊疗请遵医嘱。 |
 扫一扫
扫一扫