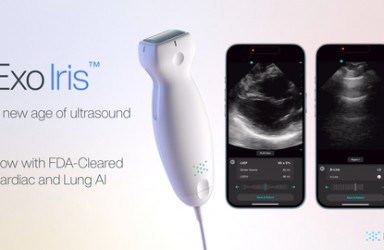
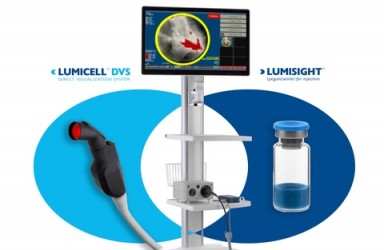
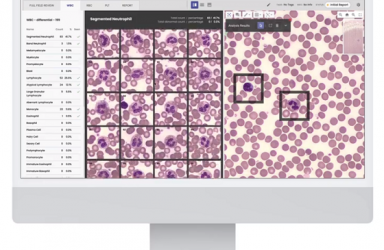
FoundationOne® CDx Cancer Genomic Profile(简称“F1CDx”,癌症基因组分析测试)。
F1CDx是由罗氏旗下癌症诊疗公司Foundation Medicine是针对所有实体瘤的综合基因组分析(CGP)测试,其中包括多种伴随诊断。是基于体外诊断的设测序设备,利用从患者肿瘤组织分离出的DNA,检测和分析多达324个基因中的替代、插入和删除改变、选定的基因重排,以及包括微卫星不稳定性(MSI)和肿瘤突变负担(TMB)在内的基因组标签(genomic signature)。
2017年11月,F1CDx作为突破性的伴随诊断产品获得美国FDA批准。FDA批准了FoundationOne CDx作为15种靶向癌症疗法的辅助诊断方法,其中包括肺癌药物奥希替尼(Tagrisso)和克唑替尼(Xalkori),卵巢癌治疗鲁卡帕利(Rubraca)和乳腺癌药物曲妥珠单抗(Herceptin) )和帕妥珠单抗(Perjeta)。
2019年6月,F1CDx在日本首次获批,F1CDx是日本批准用于检测肿瘤BRCA突变的首个伴随诊断试剂盒,可用于检测生殖系(遗传性)和体细胞(获得性)BRCA突变。
2019年09月25日,瑞士罗氏制药(Roche)控股的日本中外制药(Chugai)宣布,日本卫生劳动福利部(MHLW)批准扩大F1CDx的使用,作为阿斯利康抗肿瘤药PARP抑制剂Lynparza(olaparib)利普卓(奥拉帕利)用于BRCA突变晚期卵巢癌患者一线化疗后维持治疗的一款伴随诊断试剂盒。
此次批准,将允许医生通过采用F1CDx检测BRCA1/2基因突变,识别出在一线化疗后可能从Lynparza维持治疗中获益的BRCA突变晚期卵巢癌患者。
F1CDx在日本已被批准用于15种分子靶向药物的伴随诊断。这款试剂盒可同时检测多个获监管机构认证的临床遗传突变,超出此前“一种药物一种检测”模式。
在美国,FoundationOne® CDx 是售价为$5,800美元。

 扫一扫
扫一扫