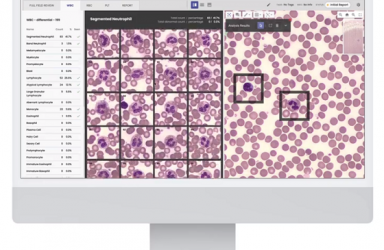
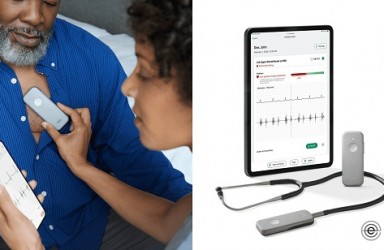
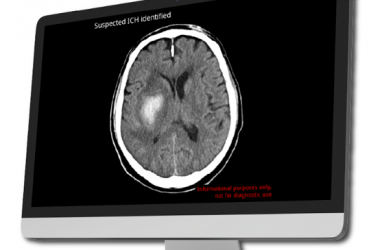
FoundationOne Liquid,基于血液的下一代测序(NGS)产品。
2019年09月29日 罗氏(Roche)旗下基因泰克近日公布了II/III期临床研究BFAST(血液首个检测筛选试验)单臂队列的阳性结果。
该研究是一项全球性、多中心、开放标签、多队列研究,正在评估靶向疗法或免疫疗法作为单药疗法或联合疗法治疗不可切除性、晚期或转移性非小细胞肺癌(NSCLC)患者的疗效和安全性,这些患者经基于血液的下一代测序(NGS)ctDNA检测确定为携带致癌体细胞突变或肿瘤突变负担(TMB)阳性。
BFAST研究是仅使用基于血液的下一代测序(NGS)来检测特异性融合的首个前瞻性研究,目的是为晚期NSCLC患者选择治疗方案,而无需组织活检。
阿来替尼(Alecensa)间变性淋巴瘤激酶(ALK)阳性队列是首个获得数据的队列,其他队列的数据之后将陆续获得。
阿来替尼(Alecensa) ALK阳性队列的主要终点是确认的调查员(INV)评估的总缓解率(ORR)
次要终点包括:
- 独立审查机构(IRF)评估的ORR
- 缓解持续时间(DoR,INV和IRF)
- 无进展生存期(PFS,INV和IRF)
- 总生存期(OS)
- 安全性
来自阿来替尼(Alecensa) ALK队列的数据显示,采用FoundationOne液体活检识别为ALK融合晚期NSCLC的患者中,经研究调查员采用实体瘤疗效评价标准(RECIST v1.1)评估,有87.4%(95%CI:78.5-93.5)的患者对Alecensa显示出确认的缓解(ORR)。
这一数据与关键性III期临床研究ALEX中观察到的阿来替尼(Alecensa)治疗的ORR一致,该研究中采用基于组织的检测分析来识别患者。
- 当独立审查委员会采用RECIST v1.1评估时,确认的ORR在数值上较高,为92%(95%CI:84.1-96.7)。
- 中位随访12.6个月,中位无进展生存期(PFS)和缓解持续时间(DOR)尚未达到。
- 该研究中, Alecensa的安全性与治疗前的临床研究和上市后经验一致,没有观察到新的安全信号。
BFAST研究采用了FoundationOne Liquid,这是罗氏旗下公司Foundation Medicine开发的一款综合性液体活组织检测产品,在来源于抽取血液的循环肿瘤DNA(ctDNA)中检测四种主要的基因组改变、微卫星不稳定性(MSI)和包括ALK在内的选择性融合。
这些数据表明,FoundationOne Liquid检测产品可以帮助测试和鉴定不适合当前诊断检测但可能受益于阿来替尼(Alecensa)的更广泛晚期NSCLC患者(例如,由于肿瘤组织不足或缺乏而不能提供组织样本的患者、或组织诊断不可用),并验证了基于血液的NGS作为一种额外方法来提示ALK阳性NSCLC临床决策的临床效果。

Alecensa(alectinib,艾乐替尼/阿来替尼)是一种靶向ALK的新型小分子酪氨酸激酶抑制剂(TKI)。
- 2015年12月,在美国获得加速批准,作为一种单药疗法,用于既往接受过Xalkori(crizotinib,克唑替尼)治疗的ALK阳性晚期NSCLC成人患者的二线治疗。
- 2017年2月,阿来替尼在欧盟获得有条件批准,作为一种单药疗法,用于既往接受过Xalkori(crizotinib,克唑替尼)治疗的ALK阳性晚期NSCLC成人患者的二线治疗。
- 2017年11月 Alecensa(alectinib,艾乐替尼/阿来替尼)获美国批准,作为单药疗法,用于ALK阳性NSCLC的一线治疗。
- 2017年12月,欧盟批准Alecensa(alectinib,艾乐替尼/阿来替尼),作为单药疗法,用于ALK阳性NSCLC的一线治疗。
- 2018年8月,阿来替尼在中国获批,作为一种单药疗法,用于ALK阳性NSCLC患者的治疗。
- 迄今为止,阿来替尼已获全球60多个国家批准,用于ALK阳性晚期NSCLC的初始(一线)治疗。
大多数ALK阳性NSCLC患者在接受当前标准护理药物克唑替尼治疗一年内会产生耐药性,大约60%会发生中枢神经系统(CNS)转移。研究显示,阿来替尼能够透过血脑屏障,在CNS中保持活性,因此该药针对脑转移瘤也具有疗效。
 扫一扫
扫一扫