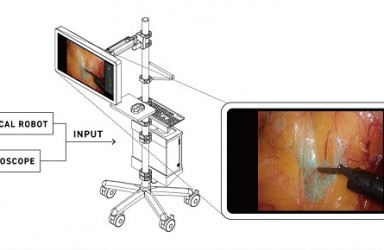
2024年04月18日-(马萨诸塞州牛顿)-专注于开发用于手术期间癌组织检测的创新荧光引导成像技术的Lumicell, Inc.公司,今天宣布美国食品和药物管理局 (FDA) 批准了公司的 LUMISIGHT™(pegulicianine)光学成像剂的新药申请 (NDA) 和 Lumicell™ 直接可视化系统 (DVS) 的上市前批准 (PMA) 申请,统称为 LumiSystem™。

LumiSystem 的诊断准确率高达 84%,使外科医生能够在肿块切除术后实时扫描乳腔,以检测和切除可能被遗漏的残留癌症,从而可能使一些患者免于二次手术。LumiSystem 组合适用于成人乳腺癌患者的荧光成像,作为肿瘤切除术中切除原发标本后术中检测切除腔内癌组织的辅助手段。
该系统的安全性是根据美国顶级学术和地区社区癌症中心的五项临床研究中超过 700 名乳腺癌患者的数据确定的。LUMISIGHT 最常见的副作用是过敏和尿液颜色异常。 LUMISIGHT 可能会引起严重的过敏反应,包括过敏反应。用于支持该系统功效的新型肿瘤切除手术成像 (INSITE) 关键试验的研究结果发表在NEJM Evidence上。
关于 Lumicell 公司
Lumicell 是一家私营公司,致力于通过推进其创新荧光引导手术技术的开发和商业化来实现更完整的癌症切除。该公司的主导产品是 LUMISIGHT™(pegulicianine)和 Lumicell™ DVS,它们设计用于在初始肿瘤切除手术期间联合使用来照亮乳腔内的癌组织,作为护理标准的辅助手段。 Lumicell 的专有泛肿瘤光学成像剂 LUMISIGHT 也正在探索针对多种实体瘤适应症的进一步开发。
| 信息 | 来源 |
| Lumicell’s Cutting-Edge Imaging Platform Receives Historic FDA Approval to Illuminate Residual Breast Cancer | https://www.businesswire.com/news/home/20240418089547/en/Lumicell%E2%80%99s-Cutting-Edge-Imaging-Platform-Receives-Historic-FDA-Approval-to-Illuminate-Residual-Breast-Cancer |
| 免责声明 | 本资料仅作参考,诊疗请遵医嘱。 |
 扫一扫
扫一扫