Novavax新冠肺炎疫苗COVOVAX™(NVX-CoV2373)是一种基于蛋白质的候选疫苗,根据第一株SARS-CoV-2(新冠肺炎致病病毒)的基因序列改造而成。NVX-CoV2373的制造采用Novavax重组纳米颗粒技术,以产生由冠状病毒刺突蛋白衍生的抗原,并采用Novavax获得专利的皂甙基Matrix-M™佐剂,以增强免疫应答和刺激产生高水平的中和抗体。NVX-CoV2373含有纯化蛋白抗原,既不能复制,也不能导致新冠肺炎。
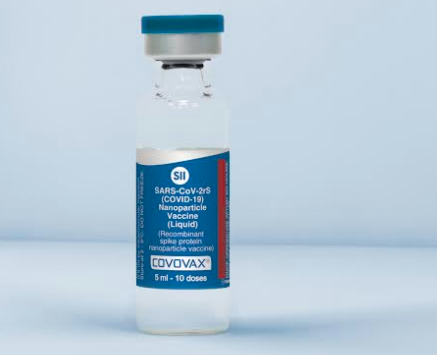
2021年11月02日(美国马里兰州盖瑟斯堡)生物技术公司Novavax,Inc.(纳斯达克股票代码:NVAX)与全球产量最大的疫苗制造商印度血清研究所私人有限公司 (SII)宣布,印度尼西亚共和国国家药品和食品控制局(Badan Peng was Obat dan Makanan(Badan POM))已授予Novavax使用Matrix-M™佐剂的重组纳米颗粒蛋白新冠肺炎疫苗COVOVAX™紧急使用授权(EUA)。
- 疫苗将由SII在印度制造,并由SII在印度尼西亚以COVOVAX™品牌上市销售。
NVX-CoV2373正在两项关键性3期试验中接受评估:在美国和墨西哥进行的PREVENT-19试验,其显示出对中重症的保护率为100%,总体有效性为90.4%。该疫苗总体耐受性良好,并产生了可靠的抗体反应。它还在英国进行了临床评估,结果表明对原始病毒株的有效性为96.4%,对阿尔法(B.1.1.7)变异株的有效性为86.3%,总体有效性为89.7%。
Novavax和SII已经在印度和菲律宾申请了Novavax新冠肺炎疫苗授权,并向世界卫生组织(WHO)提交了紧急使用清单(EUL)申请。Novavax最近还在英国、欧盟、加拿大和澳大利亚的监管机构完成了对Novavax疫苗授权的滚动申报。Novavax预计不久将向世界各地提交更多的疫苗监管申请,并将为其疫苗向世卫组织提交针对EUL的附加补充申请。Novavax预计将在今年年底前向美国FDA提交完整的信息包。
COVOVAX™新冠疫苗以即用型液体制剂的方式封装在十剂量药瓶中。疫苗接种方案要求分两次肌肉注射,间隔21天,每次0.5毫升(5微克抗原和50微克Matrix-M佐剂)。这款疫苗的储存温度为2-8摄氏度之间,可使用现有疫苗供应和冷链渠道。
Novavax基于皂苷的专利Matrix-M™佐剂可刺激抗原提呈细胞进入注射部位,增强局部淋巴结的抗原提呈,从而增强免疫反应,已显示出强力且耐受良好的效果。
| 信息 | 来源 |
| Novavax and Serum Institute of India Receive Emergency Use Authorization for COVID-19 Vaccine in Indonesia | https://ir.novavax.com/2021-11-01-Novavax-and-Serum-Institute-of-India-Receive-Emergency-Use-Authorization-for-COVID-19-Vaccine-in-Indonesia |
| 免责声明 | 本资料仅作信息分享参考,诊疗请遵医嘱。 |
 扫一扫
扫一扫