2022年12月19日(加州千橡市和法国卡斯特尔),Atara Biotherapeutics和Pierre Fabre联合宣布,欧盟委员会(EC)批准其免疫疗法Ebvallo(tabelecleucel)上市,作为单药治疗EB病毒(EBV)相关的移植后淋巴增殖性疾病(EBV+PTLD),病患包含曾至少接受过一次前期治疗的成人与2岁以上儿童患者。
- Ebvallo(tabelecleucel)全球首项获批的同种异体T细胞免疫疗法。
Ebvallo的上市申请是基于一项3期临床试验所获得的积极数据,去年底所公布的数据显示,截至2021年5月,在38例可评估患者(24例SOT后,14例HCT后)中观察到的平均客观缓解率(ORR)为50%(19/38,95% CI:33.4,66.6),包括完全缓解(CR;n=5,SOT;n=5,HCT)和部分缓解(PR;n=7,SOT;n=2,HCT)。在19例获得缓解的患者中,11例患者的缓解持续时间(DOR)超过6个月,中位缓解持续时间尚未达到。安全性方面与之前发表的数据一致,未报告新的信号或问题。未发生移植物抗宿主病(GvHD)、器官排斥、输注反应或与Ebvallo相关的细胞因子释放综合征等不良反应。
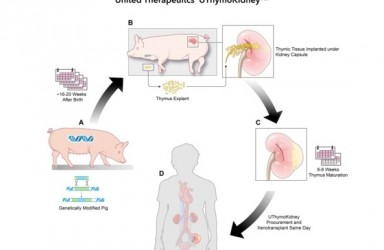
Ebvallo(tabelecleucel,tab‐cel)是一款现货型同种异体T细胞免疫疗法,以人类白细胞抗原(HLA)限定的方式靶向受EBV感染的细胞。该疗法除了针对利妥昔单抗治疗失败的移植后EBV+PTLD患者,还计划用于治疗包括鼻咽癌在内的其他EBV相关血液癌症和实体瘤。2015年2月,美国FDA授予Ebvallo用于治疗HCT后产生EBV+PTLD的突破性疗法认定(BTD)。此疗法亦获得欧盟孤儿药资格与PRIME资格。此款疗法于今年10月获得欧盟人用药品委员会(CHMP)上市许可推荐。
EB病毒(EBV)相关的移植后淋巴增殖性疾病(Epstein‑Barr virus positive post‑transplant lymphoproliferative disease,EBV+PTLD)是淋巴瘤的一种类型,是一种罕见、急性可能致死的血液癌症,可能在实体器官移植(SOT)或同种异体造血细胞移植(HCT)后发生。一线治疗失败的HCT后EBV+PTLD患者的中位总生存期为16-56天,而SOT后高危EBV+PTLD患者的1年和2年生存率分别为36%和0%。这些患者具有显著的未竟医疗需求。
| 信息 | 来源 |
| Atara Biotherapeutics’ Ebvallo™ (tabelecleucel) Receives European Commission Approval as First Ever Therapy for Adults and Children with EBV+ PTLD | https://investors.atarabio.com/news-events/press-releases/detail/301/atara-biotherapeutics-ebvallo-tabelecleucel |
| 免责声明 | 本资料仅作参考,诊疗请遵医嘱。 |
 扫一扫
扫一扫