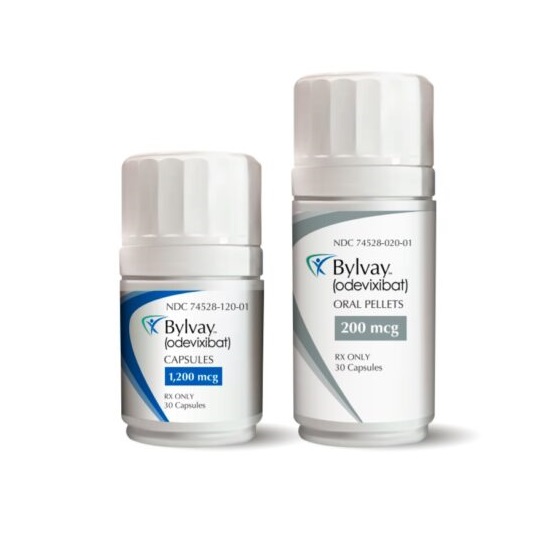
2021年07月20日,Albireo Pharma宣布美国FDA已批准Bylvay(odevixibat)上市,用于在所有亚型的进行性家族性肝内胆汁淤积(PFIC)患者中治疗瘙痒的药物。
- Bylvay是首个获批用于PFIC中治疗瘙痒的药物
Bylvay的获批得到了PEDFIC 1和PEDFIC 2两项全球性3期临床试验数据的支持。在随机双盲、含安慰剂对照的PEDFIC 1研究中,Bylvay达到了降低瘙痒(p=0.004)和血清胆汁酸(p=0.003)的主要终点,且耐受性良好,腹泻/排便频繁的发生率很低。
PEDFIC 2是一项长期、开放标签、3期扩展研究,再次证实了Bylvay在接受长达48周治疗的患者中可持续降低血清胆汁酸,并改善瘙痒评估、生长和其他肝功能标志物。
Bylvay(Odevixibat)不需要冷藏,可以每日一次以胶囊形式服用。
Bylvay(Odevixibat)A4250,是一种首创、强效选择性、非系统性、回肠胆汁酸转运体(IBAT)抑制剂,具有最小的全身暴露并在肠道内局部发挥作用。该药正被开发用于罕见儿童胆汁淤积性肝病的治疗,包括PFIC、胆道闭锁、Alagille综合征。其中,PFIC是首个目标适应症。
进行性家族性肝内胆汁淤积(Progressive Familial Intrahepatic Cholestasis,PFIC)是一种罕见的儿童疾病,导致进行性、危及生命的肝病。根据致病基因的不同,PFIC主要分为六个亚型,即PFIC1、PFIC2、PFIC3和新有学者提出的PFIC4、PFIC5和PFIC6,分别由ATP8B1、ABCB11、ABCB4、TJP2、NR1H4和MYO5B基因突变引起。
在许多情况下,PFIC在患者出生后10年内导致肝硬化和肝衰竭。PFIC最突出的持续症状是剧烈瘙痒,通常导致生活质量严重下降。此前,PFIC还没有获批的药物。只有包括胆道改道手术(biliary diversion surgery)和肝移植在内的手术选择可用,没有它们,大多数PFIC患者无法活过30岁。
 扫一扫
扫一扫