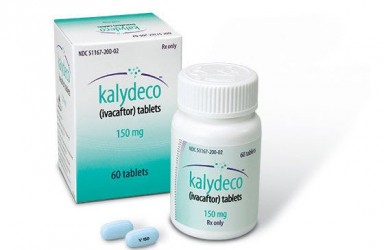
2023年05月03日-(波士顿)-Vertex Pharmaceuticals Incorporated宣布,美国食品和药物管理局 (FDA) 批准 KALYDECO ® (ivacaftor) 依伐卡托用于1个月/大于1个月的囊性纤维化 (CF) 儿童.
该批准得到了一项为期 24 周、开放标签的第 3 期队列研究的支持,该研究旨在评估 ivacaftor 在 24 个月以下且具有 ivacaftor 反应性 CFTR 突变的 CF 受试者中的安全性、药代动力学和药效学. 该队列显示出与在年龄较大的儿童和成人中观察到的相似的安全性特征。
KALYDECO ®于2012年在美国首次获得批准,现已在30多个国家上市。此前根据临床和/或体外试验数据,4个月大的婴儿囊性纤维化跨膜电导调节因子 (CFTR) 基因中至少有一处突变对 KALYDECO®有反应。KALYDECO®已在美国和欧盟获准用于治疗4个月及以上患者的囊性纤维化 (CF) 。
囊性纤维化 (Cystic Fibrosis,CF) 是一种罕见的、缩短寿命的遗传病,影响全球超过88,000 人。CF 是一种进行性多器官疾病,会影响肺、肝、胰腺、胃肠道、鼻窦、汗腺和生殖道。囊性纤维化 (CF) 是由CFTR基因中的某些突变导致的 CFTR 蛋白缺陷和/或缺失引起的。儿童必须继承两个有缺陷的CFTR基因(每个父母一个)才能患有CF,并且可以通过基因测试识别这些突变。
虽然有许多不同类型的CFTR突变可导致该疾病,但绝大多数CF患者至少有一种F508del突变。CFTR突变通过导致 CFTR 蛋白缺陷或导致细胞表面 CFTR 蛋白短缺或缺失而导致 CF。CFTR 蛋白的功能缺陷和/或缺失会导致盐和水流入和流出许多器官的细胞。在肺部,这会导致异常粘稠的粘液积聚、慢性肺部感染和进行性肺损伤,最终导致许多患者死亡。死亡年龄的中位数在30岁出头。
Kalydeco(ivacaftor)依伐卡托 在CFTR基因 发生某些类型突变的人群中,细胞表面的 CFTR 蛋白无法正常发挥作用。ivacaftor 被称为 CFTR 增效剂,是一种口服药物,旨在促进 CFTR 蛋白将盐和水转运穿过细胞膜的能力,这有助于水合物和清除呼吸道粘液。KALYDECO® (ivacaftor) 是第1种治疗CFTR基因特定突变人群囊性纤维化根本原因的药物。
| 信息 | 来源 |
| Vertex Announces U.S. FDA Approval for KALYDECO® (ivacaftor) to Treat Eligible Infants With CF Ages 1 Month and Older | https://www.businesswire.com/news/home/20230503006018/en/Vertex-Announces-U.S.-FDA-Approval-for-KALYDECO%C2%AE-ivacaftor-to-Treat-Eligible-Infants-With-CF-Ages-1-Month-and-Older |
| 免责声明 | 本资料仅作参考,诊疗请遵医嘱。 |
 扫一扫
扫一扫